免疫疗法是通过刺激机体的免疫系统,抑制和杀伤肿瘤细胞。程序性细胞死亡受体-1(PD-1)/程序性细胞死亡配体-1(PD-L1)的免疫检查点阻断治疗在临床肿瘤免疫治疗中展现出巨大的前景,但肿瘤免疫抑制微环境导致的T细胞浸润不足以及抗PD-L1抗体(αPD-L1)在肿瘤部位积累不足会造成患者低响应率和不可预测的免疫相关不良事件(irAEs),限制了肿瘤免疫疗法的进一步发展。
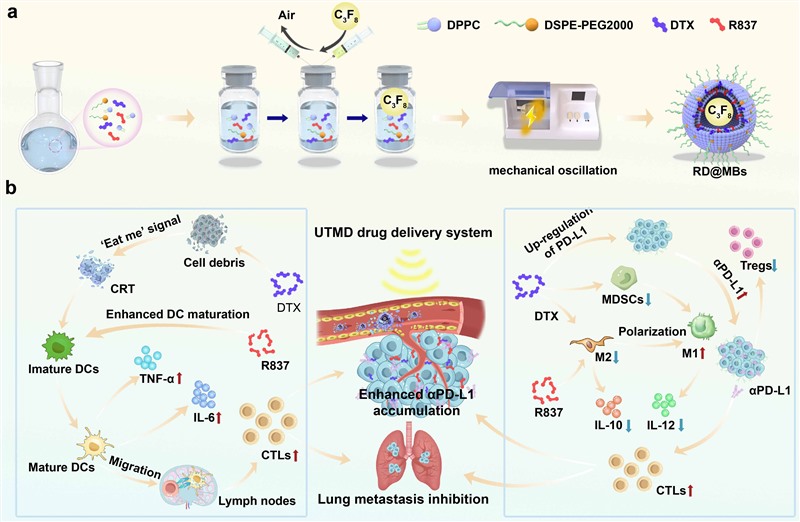
图1. RD@MBs通过调控肿瘤免疫抑制微环境和促进αPD-L1在肿瘤中的富集改善抗肿瘤免疫应答。
为了解决上述难题,我院超声科王志刚教授团队设计了一种基于超声靶向微泡破坏(UTMD)技术的药物递送系统(RD@MBs),用于调控肿瘤的免疫抑制微环境并增加αPD-L1在肿瘤中的聚集,进而提高αPD-L1的免疫检查点阻断治疗的响应率(图1)。该系统中将化疗药物多烯紫杉醇(DTX)和免疫佐剂R837载入超声微泡中。在超声辐照下,释放于肿瘤组织的DTX杀伤肿瘤细胞并释放肿瘤相关抗原和T细胞刺激因子(CRT、CD80、CD86等),激活抗肿瘤免疫反应。同时,DTX展现出强大的免疫调节能力,如通过上调肿瘤细胞表面PD-L1的表达促进αPD-L1的摄取以及诱导M0型和M2型肿瘤相关巨噬细胞向M1型的极化。此外,R837也可作为调节肿瘤相关巨噬细胞极化的调节剂,与DTX协同缓解肿瘤的免疫抑制微环境,促进T细胞的活化、增殖和向肿瘤组织的浸润,降低αPD-L1免疫检查点阻断治疗的耐药性并提高应答率。这一过程中UTMD技术的空化效应能够进一步提高肿瘤中αPD-L1的富集增效免疫检查点阻断治疗。本研究通过原位乳腺癌和皮下结直肠癌肿瘤模型证明了RD@MBs联合αPD-L1的协同治疗不仅有效抑制了原发肿瘤的生长,还显著抑制了模拟的远处转移肿瘤和肺转移瘤(图2)。RD@MBs具有较高的生物相容性、生物安全性以及调节肿瘤免疫抑制微环境的能力,因此基于RD@MBs + αPD-L1的化学免疫治疗为肿瘤的免疫检查点阻断治疗提供了新的视角。相关研究成果以标题为“Drug-loaded microbubble delivery system to enhance PD-L1 blockade immunotherapy with remodeling immune microenvironment”发表在国际知名期刊《Biomaterials Research》(IF=15.863)上。
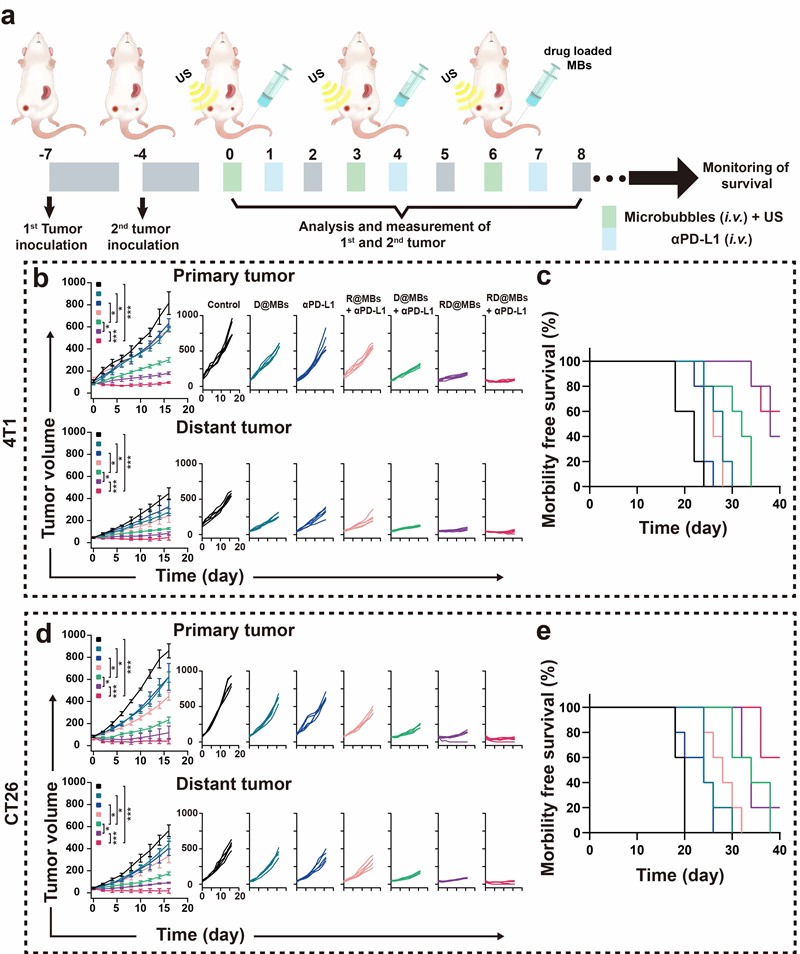
图2. RD@MBs + αPD-L1在乳腺癌和结直肠癌肿瘤模型中抗肿瘤免疫治疗。
该研究工作得到了国家自然科学基金项目、重庆市技术创新与应用发展专项重点项目、重庆市自然科学基金和中国博士后科学基金经费资助。原文链接:https://doi.org/10.1186/s40824-023-00350-5
作者:郑君
初审:黄慧哲、王志刚 复审:周青 终审:李春莉
服务热线
服务热线
版权所有: 重庆医科大学附属第二医院 | Copyright @ 2016-2026 CQSAHCQMU.CN All Right Reserved. 渝ICP备15009793号-10 渝公网安备 50010302000990号
技术支持:瑞秀科技
