重庆医科大学附属第二医院超声科任建丽教授团队长期致力于肽功能化纳米分子探针的研发、诊疗一体化多模态造影剂的制备与优化、无创性和可视化精准治疗等相关领域的基础和临床研究。近期,团队成员在肽功能化纳米系统增强声动力、声催化及逆转肿瘤耐药等方面取得系列研究成果,先后有4篇学术论文分别发表在Advanced science(JCR 1区,IF=17.521)、ACS applied materials&interface(JCR 1区,IF=10.383)、Small(JCR 1区,IF=15.153)和在Journal of Nanobiotechnology (JCR 1区,IF=9.429),重庆医科大学附属第二医院为上述论文的第一作者和通讯作者单位,超声科博士后江唯希、博士研究生郭迅、硕士研究生程晨和硕士研究生谢卓晏分别为上述论文的第一作者,任建丽教授为上述论文的通讯作者。
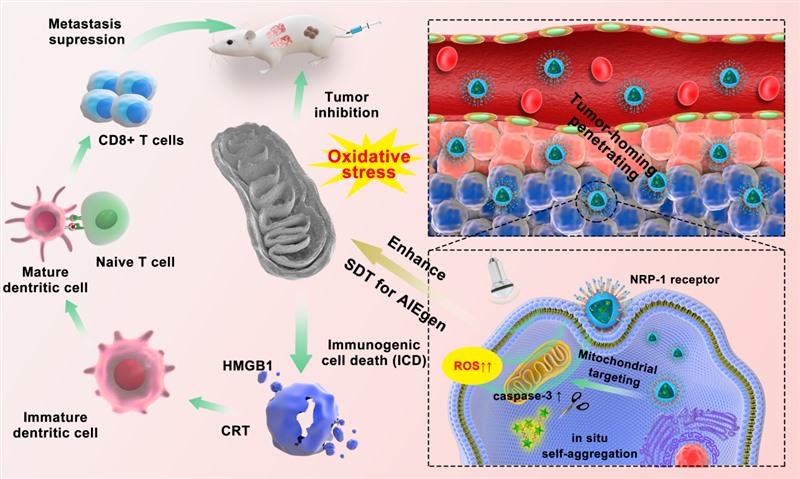
2022年12月,任建丽教授团队发表题为“Peptide supramolecular assembly-instructed in situ self-aggregation for stratified targeting sonodynamic therapy enhancement of AIE luminogens”的研究论文。运用超分子自组装的方式构建出一种多肽-AIE杂合纳米系统(peptide-AIE hybrid nanosystem,PAHN)。该纳米系统由一段包含肿瘤归巢穿膜、线粒体靶向和caspase-3响应三种功能的多肽序列与AIE分子双芘(BP)共价键合而成。在水溶液中,该化合物自组装形成粒径约10nm左右的纳米粒。经静脉注射后,纳米粒在多肽序列的介导下实现了从乳腺癌组织-癌细胞-细胞器的层层递进靶向。并且在肿瘤内上调的caspase-3的响应下,PAHN的亲水段序列从多肽中断裂脱离,使纳米粒在肿瘤内原位自聚集。接下来在组织穿透力更强的超声波辐照下,BP通过AIE效应将吸收的声能最大程度转化成ROS,从而造成肿瘤强烈的线粒体氧化应激和免疫原性死亡。
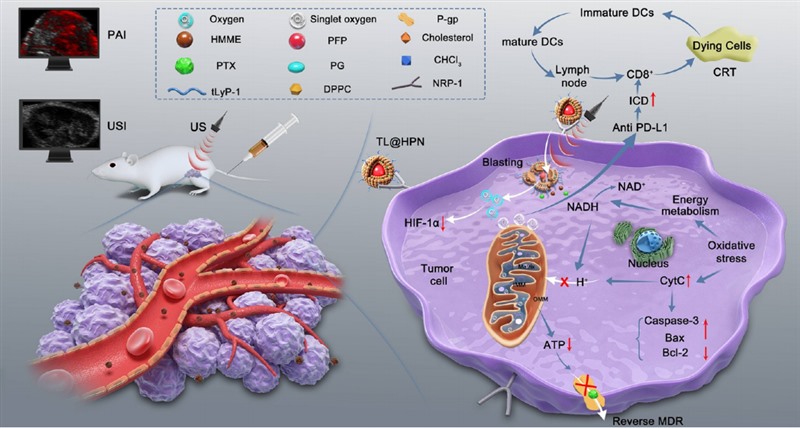
2023年1月,任建丽教授团队发表题为“Nanoenabled tumor energy metabolism disorder via sonodynamic therapy for multidrug resistance reversal and metastasis inhibition”的研究论文,报道了超声控制的纳米能量代谢干扰器对耐药乳腺癌的诊疗研究。该研究构建的纳米能量代谢干扰器借助tLyP-1多肽有效穿透乳腺肿瘤,PFP内核在超声刺激下爆破释放紫杉醇和血卟啉单甲醚,提高肿瘤细胞内药效浓度,由此放大的声动力效果精准杀伤线粒体,打破氧化还原平衡,干扰呼吸链电子传递,启动线粒体凋亡。此外,肿瘤细胞线粒体受损导致ATP产生明显受限,切断P-gp能量来源,逆转肿瘤耐药。结合该纳米能量代谢干扰器卓越的光声、超声成像能力,为耐药肿瘤诊疗一体化提供新的治疗策略。
2023年1月,任建丽教授团队发表题为"Tumor-penetrating nanoplatform with ultrasound “unlocking”for cascade synergistic therapy and visual feedback under hypoxia"的研究论文,报道了一种可视化肿瘤渗透的纳米平台,用于克服传统SDT纳米治疗的脱靶效应与不可控的氧气泄露等缺陷。该纳米平台以脂质膜为核心,用以负载GOD、H(Gd)和PFP等多种功能性材料,再加以tLyP-1肽链修饰外壳,实现了各组分的精准递送。在低强度聚焦超声辐照条件下,激活了相关材料的功能:GOD通过酶促氧化反应消耗O2和葡萄糖,产生ROS(H2O2)和葡萄糖酸,实现饥饿疗法;H(Gd) 通过消耗O2并产生ROS(1O2),实现SDT;而PFP携带的O2,可以缓解肿瘤的原位缺氧,并为其余两种治疗方式提供充足的O2供应。最终,该纳米平台不仅能够有效抑制乳腺癌小鼠模型的肿瘤进展,而且具备较高的生物安全性,这种基于纳米平台的级联工程与超声医学的交叉融合研究具有进一步临床转化的前瞻性意义。

2023年4月,任建丽教授团队发表题为"NIR activated multimodal therapeutics based on metal-phenolic networks-functionalized nanoplatform for combating against multidrug resistance and metastasis"的研究论文。该研究设计了一种“金属多酚网络功能化纳米系统”(t-P@TFP NPs),旨在实现肿瘤多种治疗方式,并在多模态成像监测下重塑肿瘤微环境从不敏感到敏感,对抗肿瘤多药耐药和转移。t-P@TFP NPs经静脉注射后,在肿瘤归巢穿膜肽介导下优先聚集到肿瘤部位,并穿透到深部肿瘤细胞中。经近红外激光辐照后激活多级反应:光热触发t-P@TFP NPs相变、破裂,释放单宁酸/铁离子包裹紫杉醇的P@TF NPs。P@TF NPs通过消耗肿瘤细胞内高含量的ATP释放PTX,抑制ATP依赖的药物外排,提高肿瘤对化疗药物的敏感性。此外,光热诱导的免疫原性细胞死亡(ICD),激发了机体免疫系统的识别功能,接着通过PD-1/PD-L1阻断,触发DC成熟,激活T细胞相关的抗肿瘤免疫应答,将免疫抑制的“冷”肿瘤转化为免疫活性的“热”肿瘤。最终,在光声、核磁、超声成像的指导下,实现光热治疗、增敏化疗和免疫治疗协同产生的三管齐下效应,克服了肿瘤耐药,抑制肿瘤转移。

近年,任建丽教授课题组依托重庆医科大学超声影像学研究所及超声分子影像重庆市重点实验室,在超声精准分子影像、肽功能化纳米分子探针用于疾病诊疗一体化领域取得了一系列高水平的研究成果,相关研究成果已在Advanced science、Small、Nano letter、Theranostics等高水平学术期刊发表,并申请相关国家发明专利4项,上述研究工作得到了国家自然科学基金面上项目的资助。
作者:超声科
初审:任建丽 复审:陆毅 终审:黄慧哲
服务热线
服务热线
版权所有: 重庆医科大学附属第二医院 | Copyright @ 2016-2026 CQSAHCQMU.CN All Right Reserved. 渝ICP备15009793号-10 渝公网安备 50010302000990号
技术支持:瑞秀科技
