2024年2月14日,重庆医科大学附属第二医院超声科任建丽教授团队在《Advanced Materials》(IF=29.4)杂志正式发表题为“Decomposable Nanoagonists Enable NIR-Elicited cGAS-STING Activation for Tandem-Amplified Photodynamic-Metalloimmunotherapy”的研究论著。本研究开发了一种基于金属有机框架(MOF)的纳米激动剂(DZ@A7),其能够响应肿瘤微环境(TME)及近红外(NIR)照射用于局部肿瘤特异性STING激活和光动力-金属免疫疗法,并在乳腺肿瘤小鼠模型中实现了原发性和转移性肿瘤生长的高效抑制。

《Advanced Materials》论文正式发表版本首页截图
纳米医学的快速发展为整合多功能疗法和免疫制剂以提高肿瘤免疫治疗效果提供了新方向。干扰素(IFN)基因的环状GMP-AMP合酶刺激因子(cGAS-STING)通路是肿瘤免疫中一个关键的先天免疫激活途径。cGAS-STING通路激活可以上调I型IFN和促炎细胞因子的分泌,触发宿主免疫反应以增强治疗效果。将天然环状二核苷酸(CDN)和小分子等STING激动剂制作成纳米制剂,能够改善其代谢不稳定和生物利用度低的缺点。但该策略依赖高剂量给药,往往因过度释放或激动剂不受控释放导致非靶细胞的非预期激活。近期,新的证据揭示了金属离子在促进cGAS-STING信号转导中的重要作用,提供了一种结合STING激活和纳米治疗实现金属免疫疗法的替代策略。该研究开发了一种基于金属有机框架(MOF)的纳米激动剂(DZ@A7),其能够响应肿瘤微环境(TME)及近红外(NIR)照射,用于局部肿瘤特异性STING激活和光动力-金属免疫疗法。
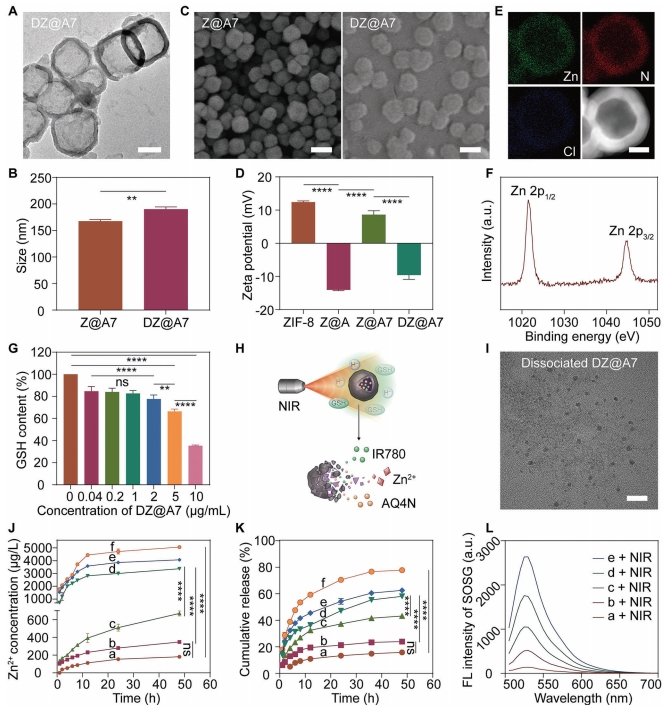
图1 DZ@A7纳米激动剂制备及响应性降解
一方面,通过聚多巴胺介导的细胞内谷胱甘肽消耗,DZ@A7能够在NIR照射下加剧线粒体原位氧化应激损伤,显著促进线粒体DNA的释放。此外,乏氧响应性药物AQ4N可通过抑制细胞核DNA的修复进一步增强细胞质受损DNA的积累,从而激活cGAS-STING途径。另一方面,DZ@A7特异性降解导致肿瘤细胞内Zn2+超载,提高cGAS酶活性,加速其对胞质受损DNA的识别以启动STING途径。
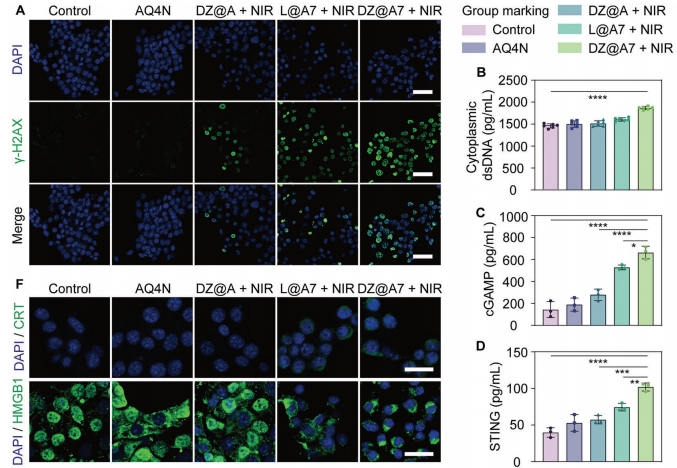
图2 NIR照射DZ@A7诱导肿瘤免疫原性死亡和STING激活
光敏剂IR780可以通过在大多数类型肿瘤细胞中过表达的有机阴离子转运多肽进行转运,从而表现出结构上固有的肿瘤靶向性,保证了DZ@A7在肿瘤组织的优先积累和特异性Zn2+超载。纳米激动剂介导的光动力-金属免疫治疗在小鼠体内明显上调STING信号,促进细胞因子和IFN-β的分泌,从而诱导DC成熟和CD8+ T细胞浸润,最终建立长期抗肿瘤免疫反应。此外,我们在乳腺癌原发性和转移性模型上都观察到高效的肿瘤生长抑制。

图3 DZ@A7的体内分布及抗肿瘤疗效评价
鉴于NIR在该治疗策略中不可或缺的作用,不同于已有纳米平台中STING激动剂的“恒定活性”药理学效应,NIR引发的纳米激动剂在抗肿瘤免疫和cGAS-STING激活途径方面为肿瘤光动力-金属免疫治疗提供了范例。

图4 纳米激动剂设计原理和可降解成分串联增强光动力-金属免疫治疗
重庆医科大学附属第二医院超声科博士研究生郭迅、博士研究生王晓婷、硕士研究生杜翅迩及重庆医科大学附属妇女儿童医院超声科涂鹏博士为本论文共同第一作者,重庆医科大学附属第二医院任建丽教授、上海大学陈雨教授及陈良副教授为共同通讯作者。本研究受国家自然科学基金面上项目的资助和支持。
作者:任建丽
初审:黄慧哲 陈芸霖 复审:陈欣 终审:李春莉
服务热线
服务热线
版权所有: 重庆医科大学附属第二医院 | Copyright @ 2016-2026 CQSAHCQMU.CN All Right Reserved. 渝ICP备15009793号-10 渝公网安备 50010302000990号
技术支持:瑞秀科技
