2024年8月26日,国家纳米科学中心王海研究员、聂广军研究员联合重庆医科大学附属第二医院冉海涛教授、谭米肖副研究员在《Nature Nanotechnology》期刊上正式发表了题为“Metal Ion-Chelated Phenylalanine Nanostructures Reverse Immune Dysfunction and Sensitize Breast Tumor to Immune Checkpoint Blockade”的基础研究文章(IF:38.1)。

《Nature Nanotechnology》论文正式发表首页截图
随着以CTLA-4、PD-1及PD-L1为代表的免疫检查点抑制剂在肿瘤中展现出显著的治疗效果,并相继获得FDA批准用于多种肿瘤的治疗,但大部分患者对其疗效有限,部分患者甚至产生耐药性。因此,如何进一步提升免疫疗效并逆转肿瘤的免疫抑制微环境,成为肿瘤免疫治疗领域的重要研究方向。
为解决这一难题,国家纳米科学中心王海研究员、聂广军研究员联合重庆医科大学附属第二医院冉海涛教授、谭米肖副研究员,构建了一种金属离子螯合的L-苯丙氨酸纳米复合物,能够精准激活树突状细胞(DC细胞)中的Kv1.3钾离子通道,并通过结合短期饥饿饮食和PD-L1免疫检查点抑制剂治疗,有效重塑肿瘤的免疫抑制微环境,显著增强了肿瘤免疫治疗的疗效。相关研究成果以“Metal Ion-Chelated Phenylalanine Nanostructures Reverse Immune Dysfunction and Sensitize Breast Tumor to Immune Checkpoint Blockade”为题,发表在《自然-纳米技术》(Nature Nanotechnology)期刊上(https://doi.org/10.1038/s41565-024-01758-3)。
DC细胞疗法:肿瘤免疫治疗新希望
作为机体免疫应答的“启动器”,DC细胞在肿瘤免疫治疗中展现出巨大潜力。它们不仅能够激发机体免疫系统,恢复肿瘤的免疫监视功能,还能与其他免疫细胞协同作战,对肿瘤免疫治疗做出重要贡献。DC细胞的功能不仅与病原体相关分子模式 (PAMP) 和危险相关分子模式 (DAMP) 信号有关,还受到电生理反应的调控。DC细胞质中的钾离子(K+)与钙离子(Ca2+)浓度与DC细胞的成熟密切相关。基于这一发现,研究团队构建了金属离子螯合的L-苯丙氨酸纳米复合物,能够精准激活DC细胞的Kv1.3钾离子通道,诱导炎症小体NLRP3信号通路和核因子-κB (NF-κB) 通路的活化,促发炎性细胞因子的分泌,进而逆转肿瘤的免疫抑制微环境,增强PD-L1免疫检查点抑制剂的治疗效果。
短期饥饿饮食:增强DC细胞疗法的效能
短期饥饿(STS)饮食是一种通过周期性禁食和进食调节饮食摄入的模式,能够激活免疫系统,并与化疗、激素疗法等肿瘤治疗方法产生协同抗肿瘤效果。研究表明,将STS饮食与金属离子螯合的L-苯丙氨酸纳米复合物介导的DC细胞疗法结合使用,能够重编程DC细胞的新陈代谢,进一步增强其抗肿瘤免疫功能。研究团队通过多种转基因鼠模型验证了这一生物学机制,为DC细胞肿瘤疫苗及DC细胞免疫疗法的临床应用提供了重要参考,展望未来,DC细胞疗法有望为肿瘤治疗带来全新希望。
重庆医科大学附属第二医院谭米肖副研究员、哈尔滨工业大学曹国梁博士为该论文共同第一作者;冉海涛教授、聂广军研究员及王海研究员为共同通讯作者。上述研究工作得到了国家自然科学基金、中科院战略性先导科技专项和国家纳米科学中心启动基金等项目的支持。
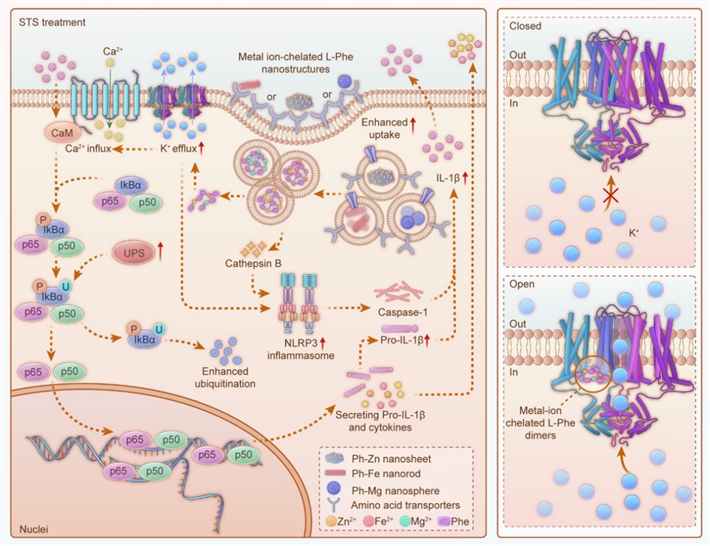
图1. 金属离子螯合的L-苯丙氨酸纳米复合物介导的DC细胞疗法联合STS饮食增效肿瘤免疫治疗示意图
服务热线
服务热线
版权所有: 重庆医科大学附属第二医院 | Copyright @ 2016-2026 CQSAHCQMU.CN All Right Reserved. 渝ICP备15009793号-10 渝公网安备 50010302000990号
技术支持:瑞秀科技
