近年来肠道微生物菌群(microbiota)在糖尿病及其微血管并发症的发生和发展中的作用引起了越来越多学者的关注。正常的肠道黏膜屏障由肠粘膜上皮细胞及上皮细胞间的紧密连接蛋白构成的机械屏障以及化学屏障、免疫屏障和微生物屏障组成,可以有效的阻挡肠道内多种、高浓度的肠道内寄生菌及其毒素的侵害。在糖尿病中,由于肠道屏障的受损和通透性增加,许多致病性的细菌及其代谢产物(例如病原体相关性分子)可通过肠道进入循环,进而产生系统性的影响,包括慢性的低度炎症、脂代谢紊乱及胰岛素抵抗。但肠道屏障受损及微生物代谢产物进入血循环后对远端靶器官及微血管并发症进展的影响及其机制尚不明确。
重庆医科大学附属第二医院内分泌科青年医生段雅倩,在美国印第安纳大学医学院(Indiana University, School of Medicine)读博期间,跟随导师(Dr. Maria Grant)致力于糖尿病视网膜微血管损伤相关机制研究,通过整合生理学的角度探索骨髓干/前体细胞与微生物肠道菌群及视网膜病变的相关性及分子机制。

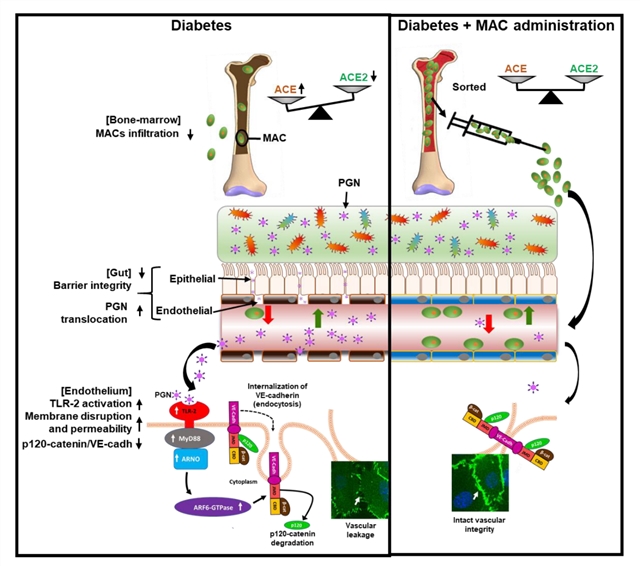
2019年10月15日,其在Circulation Research(IF=15.862)发表题为“Bone Marrow-Derived Cells Restore Functional Integrity of the Gut Epithelial and Vascular Barriers in a Model of Diabetes and ACE2 Deficiency”的研究论文,该研究首次报道从小肠中分离的有促血管生成作用的骨髓衍生前体细胞(Myeloid Angiogenic Cells)对肠道粘膜的重要保护作用。该文更进一步揭示了糖尿病小鼠中Myeloid Angiogenic Cells的缺乏导致肠道血管及内皮屏障的受损,进而使肠道菌群病原体相关性分子peptidoglycan进入循环,最终通过TLR-2介导的MyD88-ARNO-ARF6信号通路致视网膜微血管损伤。

近年来,在我院各级部门的大力支持下,内分泌科近年来大力引进国内外优秀青年人才,鼓励及支持青年医师发挥各自所长,致力于开展内分泌相关的科研创新及成果的临床转化。
全文链接:https://www.ahajournals.org/doi/abs/10.1161/CIRCRESAHA.119.315743
撰稿:段雅倩
审核:刘东方
服务热线
服务热线
版权所有: 重庆医科大学附属第二医院 | Copyright @ 2016-2026 CQSAHCQMU.CN All Right Reserved. 渝ICP备15009793号-10 渝公网安备 50010302000990号
技术支持:瑞秀科技
